Страница: 27/38
4.3. Третичная структура
Под этим термином понимают полную укладку в простанстве всей полипептидной цепи, включая укладку боковых радикалов. Полное представление о третичной структуре дают координаты всех атомов белка. Благодаря огромным успехом рентгеноструктурного анализа такие данные, за исключением координат атомов водорода получены для значительного числа белков. Это огромные массивы информации, хранящиеся в специальных банках данных на машиночитаемых носителях, и их обработка немыслима без применения быстродействующих компьютеров. Полученные на компьютерах координаты атомов дают полную информацию о геометрии полипептидной цепи, в том числе значения торсионных углов, что позволяет выявить спиральную структуру, b-складки или нерегулярные фрагменты. Примером такого исследовательского подхода может служить следующая пространственная модель структуры фермента фосфоглицераткиназы:
 |
Общая схема строения фосфоглицераткиназы. Для наглядности a-спиральные участки представлены в виде цилиндров, а b-складки – в виде лент со стрелкой, указывающей направление цепи от N-конца к С-концу. Линии – нерегулярные участки, соединяющие структурированные фрагменты.
Изображение полной структуры даже небольшой белковой молекулы на плоскости, будь то страница книги или экран дисплея мало информативно из-за чрезвычайно сложного строения объекта. Чтобы исследователь мог наглядно представлять простанственное строение молекул сложных веществ, используют методы трехмерной компьютерной графики, позволяющей выводить на дисплей отдельные части молекул и манипулировать с ними, в частности поворачивать их в нужных ракурсах.
Третичная структура формируется в результате нековалентных взаимодействий (электростатические, ионные, силы Ван-дер-Ваальса и др.) боковых радикалов, обрамляющих a-спирали и b-складки, и непериодических фрагментов полипептидной цепи. Среди связей, удерживающих третичную структуру следует отметить:
а) дисульфидный мостик ( – S – S – )
б) сложноэфирный мостик (между карбоксильной группой и гидроксильной группой)
в) солевой мостик (между карбоксильной группой и аминогруппой)
г) водородные связи.
В соответствии с формой белковой молекулы, обусловленной третичной структурой, выделяют следующие группы белков:
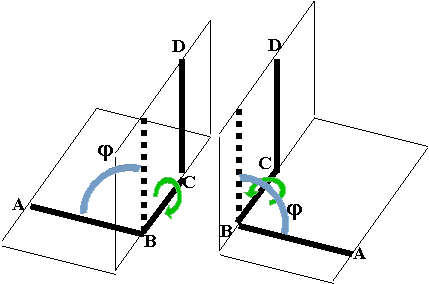
В такой системе возможен случай, когда связи А-В и С-D расположены параллельно и находятся по одну сторону от связи В-С. Если рассматривать эту систему вдоль связи В-С, то связь А-В как бы заслоняет связь C-D, поэтому такая конформация называется заслоненной. Согласно рекомендациям международных союзов химии IUPAC (International Union of Pure and Applied Chemistry) и IUB (International Union of Biochemistry), угол между плоскостями ABC и BCD считается положительным, если для приведения конформации в заслоненное состояние путем поворота на угол не выше 180° ближнюю к наблюдателю связь нужно поворачивать по часовой стрелке. Если эту связь для получения заслоненной конформации нужно поворачивать против часовой стрелки, то угол считается отрицательным. Можно заметить, что это определение не зависит от того, какая из связей находится ближе к наблюдателю.
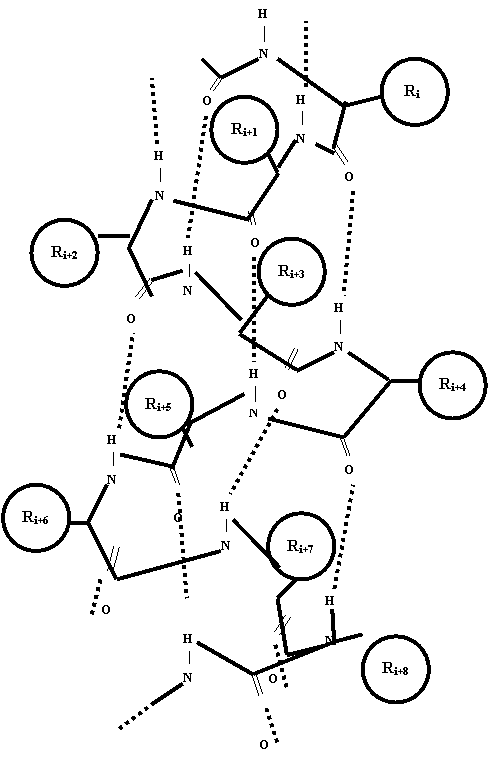
При этом, как видно из рисунка, ориентация фрагмента, содержащего атомы Ci-1a и Cia [(i-1)-й фрагмент], и фрагмента, содержащего атомы Cia и Ci+1a (i-й фрагмент), определяется торсионными углами, соответствующими вращению вокруг связи Ni¾Cia и связи Cia¾Cik. Эти углы принято обозначать как j и y, в приведенном случае соответственно ji и yi. Их значениями для всех мономерных звеньев полипептидной цепи в основном определяется геометрия этой цепи. Никаких однозначных величин ни для значения каждого из этих углов, ни для их комбинаций не существует, хотя на те и на другие накладываются ограничения, определяемые как свойствами самих пептидных фрагментов, так и природой боковых радикалов, т.е. природой аминокислотных остатков.
Реферат опубликован: 3/06/2006