Страница: 19/38
Хиломикроны являются наиболее крупными из липопротеидов и содержат до 98-99% липидов и только 1-2% белка. Они образуются в слизистой оболочки кишечника и обеспечивают транспорт липидов из кишечника в лимфу, а затем в кровь.
В ЛПНП количество белка составляет 9-20% , а среди липидов преобладают холестерин и триацилглицерины (до 40%). Белковая часть ЛПВП колеблется в пределах 35-50%, а белковая представлена фосфолипидами и холестерином. Таким образом, холестерин транспортируется по крови в составе липопротеидов, особенно ЛПНП.
Глава 7. Методы исследования белков
Среди методов, используемых в биохимии, ключевое значение имеют выделение веществ из биологических источников и, как правило, их очистка с целью получения индивидуальных соединений.
Следует отметить три главные проблемы выделения в индивидуальном виде компонентов из живых организмов:
1) Исходный материал - биомасса состоит из многих сотен и даже тысяч различных соединений. Разделение таких смесей чрезвычайно сложно, кроме того многие компоненты этих смесей построены довольно однотипно (например, иммуноглобулины). В связи с этим они мало различаются между собой по физико-химическим характеристикам - растворимости или способности к сорбции на определенном типе сорбента.
2) Работа с биохимическими объектами зачастую сопровождается необходимостью манипулировать с очень небольшими количествами исходного вещества. При ничтожно малом количестве используемого материала методы их детекции должны быть высокочувствительными. Такими методами являются спектрофотометрические методы, основанные на измерении поглощения видимого или ультрафиолетового света, радиохимические методы, основанные на изменении радиоактивности, и люминесцентные, основанные на изменении флуоресценции, био- и хемилюминесценции.
|
![]()
![]()
![]()
![]() H CH H CH
H CH H CH
|
|
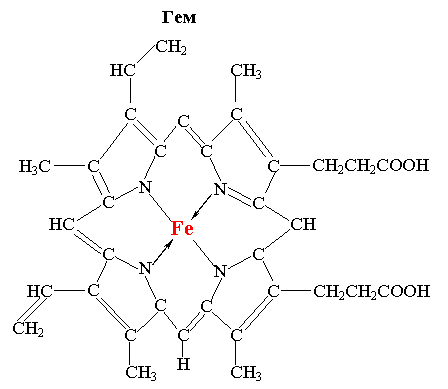
При взаимодействии молекулярного кислорода с гемоглобином существует небольшая, но конечная вероятность окисления последнего: молекула O2 не присоединяется, но окислит железо: Fe2+ + O2 Þ Fe3+ + O2–. Поэтому при дыхании в эритроцитах непрерывно образуется метгемоглобин. Для его восстановления в эритроците существует специальная ферментативная система, восстанавливающая метгемоглобин и превращающая его в нормальный дезоксигемоглобин. При нарушении этой системы возникает тяжелое заболевание – метгемоглобинемия, при которой гемоглобин перестает быть переносчиком кислорода.
Реферат опубликован: 3/06/2006